これだけは覚えていってください。「密栓NG」の例外
以前の記事でも触れたように、例外は試験に出やすいです。
今回はその中でも、「密栓してはいけない危険物」という、出題頻度が高い例外をご紹介します。
- 第5類「自己反応性物質」:エチルメチルケトンパーオキシド
- 第6類「酸化性液体」:過酸化水素
この2つは、**他の危険物と異なり“密栓してはいけない”**という例外です。
なぜなら——
密栓NGの理由:「内圧上昇で爆発の危険」
基本的に危険物は揮発や流出を防ぐため密栓保管が原則ですが、
この2つの危険物に限っては、密栓することで逆に危険が高まるのです。
- エチルメチルケトンパーオキシドや過酸化水素は時間と共に分解し、
- その際に酸素や熱を発生させてしまいます。
- 密閉容器内でこのガスがたまると、内圧が上昇→容器破裂の恐れが生じます。
言い換えると、「逃げ道がない=爆発予備軍」という状態になるわけです。
イメージは「ドライアイス爆弾」
例えるなら、ちょっと前に話題になったドライアイス爆弾と同じ原理です。
- ペットボトルに水+ドライアイス(固体の二酸化炭素)を入れる
- ドライアイスが昇華(固体→気体)して二酸化炭素に変わる
- 内部の気体が増えていき、容器が耐えられなくなり爆発!
同様に、分解反応で酸素などが発生する危険物を密栓するのは非常に危険なんです。
以下が内圧上昇による容器破壊のイメージです。
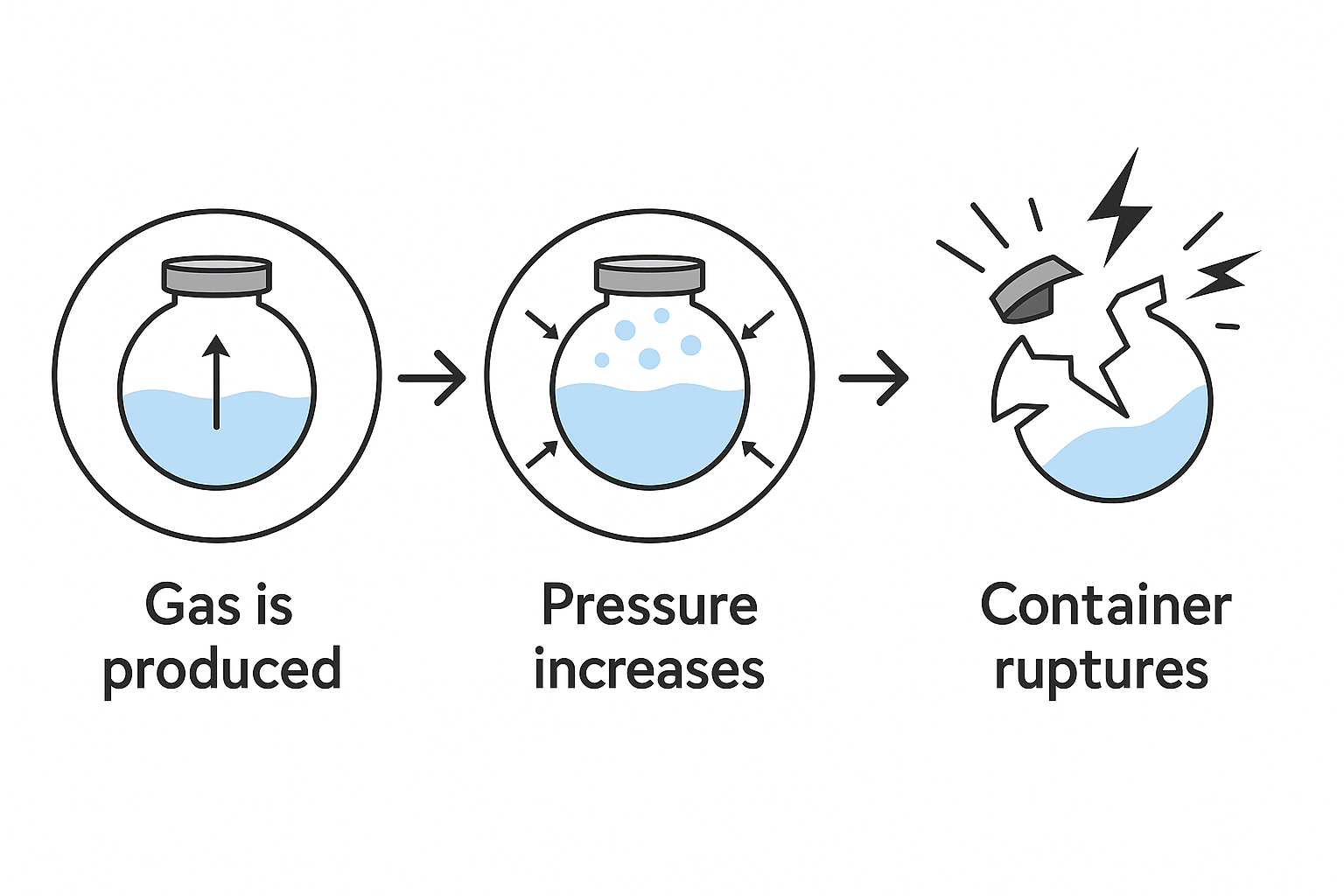
【脱線トーク】アルコールや有機溶剤は密栓OKなの?
ここでふと気になりませんか?
「じゃあ、アセトンとかエタノールみたいな揮発性の液体も内圧上がるのでは? 密栓ダメなんじゃ?」
答えは:基本的には密栓OKです。
なぜかというと、アルコールや有機溶剤は分解反応でガスを発生するわけではないからです。
これらは単なる状態変化(液体 → 気体)なので、一定条件で蒸気圧平衡が成り立つんです。
蒸気圧と平衡のはなし(物理化学とリンク!)
密栓容器内では、揮発した蒸気と液体が平衡状態になります。
この状態では、
- 一部の液体が気体になり…
- 同時に、気体が液体に戻る…
という動きがバランスを取るので、それ以上内圧は上がりません。
ただし!
- 容器が高温にさらされる
- 長期的に振動や圧力がかかる
などの条件が加わると、平衡が崩れて破裂するリスクはゼロではありません。
なので、冷暗所で密栓保管が推奨されているのです。
除光液(アセトン)で考えるとわかりやすい!
除光液の成分(アセトンや酢酸エチル)も危険物の仲間です。
ふたを開けっぱなしにしておくと、気化してどんどんなくなっていきますよね?
でも、密栓しておけばある程度揮発した段階で平衡になるので、それ以上気体が増えず、保存状態が安定します。
「密栓NG」は“分解してガスを出す”から!
まとめると…
| 危険物 | 密栓の扱い | 理由 |
|---|---|---|
| エチルメチルケトンパーオキシド | ❌ | 分解 → 酸素発生 → 内圧上昇 |
| 過酸化水素 | ❌ | 酸素発生で内圧上昇 |
| アセトン・エタノールなど | ⭕️ | 単なる揮発 → 蒸気圧平衡 |
こういう**「なぜそうするのか」**を理解しておくと、試験にも現場にも役立ちます。
最後に:物理化学分野との相性バツグン!
この話題には、
- 蒸気圧
- 平衡状態
- 状態変化
- 分解反応
といった物理化学のキーワードが満載です。
つまり、「密栓NGの例外」は法令問題にも物理化学にもつながる知識。
今のうちにここでまとめて理解しておけば、一石二鳥で得点源にできますよ!
❗ポイント復習
- 第5類&第6類の「密栓してはいけない」例外を覚える
- ドライアイス爆弾の原理と比較すると覚えやすい
- 蒸気圧と平衡の理解は物理化学分野にもつながる!




コメント